Chez Advicenne, nous nous engageons à développer un portefeuille robuste, précieux et durable de produits qui répondent aux besoins non satisfaits en matière d’options thérapeutiques pour les maladies rares.
Notre produit phare ADV7103 est aujourd’hui développé pour le traitement de deux indications, l’acidose tubulaire rénale distale (ATRd) aux Etats-Unis et la cystinurie en Europe et aux Etats-Unis.
ADV7103 pour l’ATRd
L’ADV7103 est un médicament expérimental conçu pour traiter l’acidose tubulaire rénale distale (ATRd) chez les enfants et les adultes. L’ATRd peut avoir une origine génétique, également appelée ATRd primaire, ou être acquise à la suite de troubles auto-immuns ou d’autres pathologies. Alors que la forme héréditaire de l’ATRd est plus fréquente chez les nourrissons et les enfants, la forme acquise est plus répandue chez les adultes.
L’ATRd se caractérise par une capacité réduite du rein à sécréter des protons (acides) dans l’urine, ce qui entraîne un déséquilibre du pH sanguin susceptible de provoquer des complications graves et à long terme. Celles-ci comprennent des lésions rénales, un retard de croissance et un rachitisme chez les enfants, une série de troubles métaboliques ou une altération de la fonction rénale.
Deux prises par jour
Aux Etats-Unis, la Food and Drug Administration (FDA) a approuvé la demande d’autorisation d’essai clinique de l’ADV7103 en tant que nouveau médicament de recherche (IND), permettant ainsi le lancement de l’essai pivot de phase III (ARENA-2) pour le traitement de l’ATRd. Il n’existe actuellement aucun traitement approuvé pour l’ATRd aux Etats-Unis.
L’étude a également reçu l’autorisation d’essai clinique de l’Agence de Santé Canadienne.
ADV7103 est un produit oral innovant dont la formulation est conçue pour maintenir une libération prolongée sur une période de 12 heures, permettant ainsi un traitement deux fois par jour. Le produit a été développé sous la forme d’une formulation multiparticulaire en granules de 2mm qui contient deux ingrédients pharmaceutiques actifs.
Cystinurie
Au-delà de l’ATRd, Advicenne développe également ADV7103 dans une deuxième indication, la cystinurie, une autre maladie rénale rare.
ADV7103 a reçu l’autorisation de l’Agence de Santé française (ANSM) et de l’Agence de Santé belge (AFMPS) pour initier un essai clinique pivot de Phase II/III dans la cystinurie (étude CORAL).
L’essai a été conçu pour évaluer l’efficacité, la sécurité, la tolérance et l’observance du ADV7103 chez les patients atteints de cystinurie. Il n’existe actuellement aucun traitement approuvé pour la cystinurie en Europe ou aux Etats-Unis.
Portefeuille de produits en développement
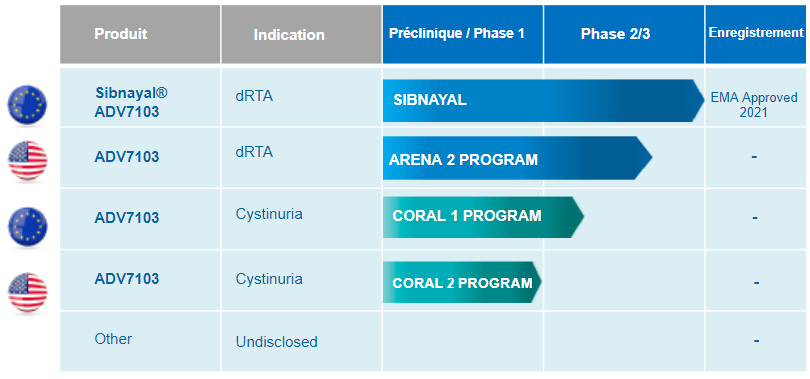
ARENA: Alkalinisation for RENal Acidosis; CORAL: Cystine – ORnithine – Arginine – Lysine (4 dibasic amino-acids for which gastro-intestinal absorption and renal reabsorption are defective in cystinuria patients